Har du nogensinde undret dig over, hvorfor salt opløses så let i vand, eller hvordan din krop sender elektriske signaler til musklerne? Svaret ligger i ioner.
Definition: Atomer med elektrisk ladning
 Et atom er i udgangspunktet neutralt, fordi det har lige mange positive protoner i kernen som negative elektroner, der bevæger sig rundt om kernen.
Et atom er i udgangspunktet neutralt, fordi det har lige mange positive protoner i kernen som negative elektroner, der bevæger sig rundt om kernen.Et ion opstår, når et atom enten afgiver eller optager en eller flere elektroner. Så bliver regnskabet ubalanceret, og atomet får en elektrisk ladning.
To typer ioner
Vi deler ioner op i to hovedgrupper baseret på deres ladning:
Positive ioner (Kationer): Opstår når et atom afgiver elektroner. Da der nu er flere protoner end elektroner, bliver ladningen positiv. (Eksempel: Magnesium, Mg2+).
Negative ioner (Anioner): Opstår når et atom optager elektroner. Da der nu er flere elektroner end protoner, bliver ladningen negativ. (Eksempel: Chlorid,Cl-).
Hvorfor sker det? (Oktetreglen)
Naturen søger stabilitet. De fleste atomer "ønsker" at fylde deres yderste elektronskal, så de har otte elektroner (ligesom ædelgasserne). Dette kaldes oktetreglen (eller otte-reglen).
- Atomer med få elektroner i yderste skal (som metaller) foretrækker at give dem væk.
- Atomer med en næsten fyldt yderskal (som ikke-metaller) foretrækker at optage elektroner.
Ionbinding: Hvordan salt bliver til
Når en positiv ion og en negativ ion mødes, sker der noget spændende: De tiltrækker hinanden som magneter. Denne kraft kaldes en ionbinding.
Det mest kendte eksempel er almindeligt bordsalt (Natriumchlorid, NaCl):
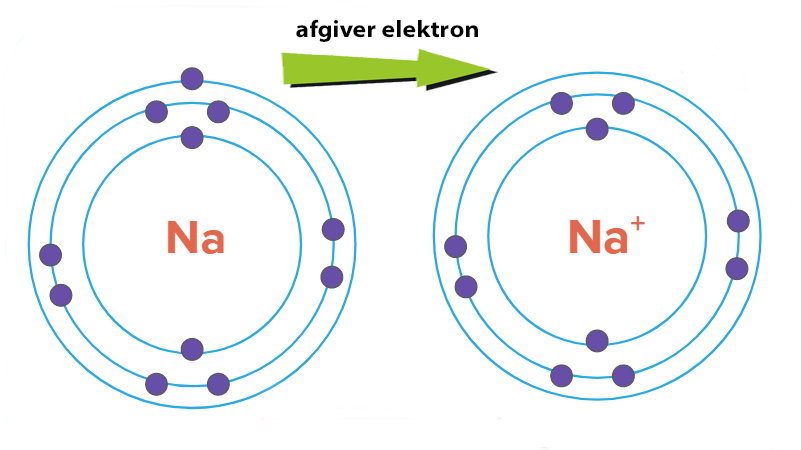
- Natrium (Na) afgiver én elektron og bliver til Na+
.
- Chlor (Cl) modtager denne elektron og bliver til Cl-
.
- De to modsatte ladninger holder dem sammen i et fast krystalgitter.
| Navn | Formel |
| Aluminat | AlO2− |
| Ammonium | NH4+ |
| Apatit | Ca5(PO4)3− |
| Arsenat | AsO43− |
| Arsenit | AsO33− |
| Azid | N3− |
| Bicarbonat | HCO3− |
| Bisulfat | HSO4− |
| Bisulfit | HSO3− |
| Borate | BO33− |
| Bromat | BrO3− |
| Bromid | Br− |
| Bromit | BrO2− |
| Carbid | C4− eller C22− |
| Carbonat | CO32− |
| Chlorat | ClO3− |
| Chlorit | ClO2− |
| Chromat | CrO4− |
| Chromit | CrO2− |
| Cyanat | CNO− |
| Cyanid | CN− |
| Dichromat | Cr2O72− |
| Dihydrogenphosphat | H2PO4− |
| Disulfid | S22− |
| Fluorid | F− |
| Hydrid | H− |
| Hydrogencarbonat | HCO3− |
| Hydrogenphosphat | HPO42− |
| Hydrogenphosphit | HPO32− |
| Hydrogensulfat | HSO4− |
| Hydrogensulfit | HSO3− |
| Hydroxid | OH− |
| Hypobromit | BrO− |
| Hypochlorit | ClO− |
| Hypoiodit | IO− |
| Hypophosphit | PO23− |
| Iodat | IO3− |
| Iodid | I− |
| Iodit | IO2− |
| Molybdat | MoO4− |
| Nitrat | NO3− |
| Nitrid | N3− |
| Nitrit | NO2− |
| Oxalat | C2O42− |
| Oxid | O2− |
| Oxonium | H3O+ |
| Perbromat | BrO4− |
| Perchlorat | ClO4− |
| Periodat | IO4− |
| Permanganat | MnO4− |
| Peroxid | O22− |
| Phosphat | PO43− |
| Phosphid | P3− |
| Phosphit | PO33− |
| Pyrophosphat | P2O74− |
| Selenat | SeO42− |
| Selenit | SeO32− |
| Silikat | SiO32− |
| Sulfat | SO42− |
| Sulfid | S2− |
| Superoxid | O2− |
| Tetrathionat | S4O62− |
| Thiocyanat | CNS− |
| Thiosulfat | S2O32− |
| Uranyl | UO32− |
| Vanadat | VO32− |
