Svarskema
| Indikator | Saltsyre | Vand (pH=7) | Natriumhydroxid |
| phenolphtalein | farveløs | gul | gul |
| Metylrødt | rød | gul | gul |
| bromthymolblåt | gul | grøn | blå |
| Indikator | Farveskift | Omslagsområde pH | pKs(Ind.) |
| Metylrødt | Rød-gul | 4,4-6,2 | 5,0 |
| bromthymolblåt | Gul-blå | 6,0-7,6 | 7,3 |
| phenolphtalein | Farveløs-rød | 8,2-10,0 | 9,7 |
De tre nævnte syre-base-indikatorer hører til de mest brugte, men i kemiske tabelværker kan man finde omslagsområderne for yderligere et stort antal indikatorer.
En indikator er en svag syre eller en hermed korresponderende svag base.
Methylrødt er således en svag syre, der reagerer med vand efter skemaet.

Forenklet kan skemaet opskrives således
lnH + H2O = ln-+ H3O+
Indikatorens sure form er rød (InH = rød), og dens korresponderende basiske form er gul (ln- = gul)
Anvendes massevirkningsloven på ligevægt, fås:
![]()
Hvor Ks(inH) er indikatorens syrestyrkekonstant
Isoleres [H3O+], fås
![]()
Koncentrationsforholdet mellem indikatorerens sure og basiske form afhænger således på meget simpel måde af opløsningens H3O+-koncentration. Tages logaritmen på venstre og højre side, kan ligningen omformes til:
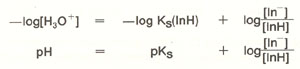
Når pH = pKs er koncentrationerne af lnH og ln- lige store, og vi har en blandingsfarve. Først når koncentrationen af den ene form bliver ca. 10 gange større end den anden, opleves farven som "ren". Det betyder pga. den logaritmiske afhængighed, at omslagsområdet for en indikator normalt strækker sig over 2 pH-enheder nemlig fra
![]()
For methylrødt finder omslaget "teoretisk" sted fra pH = 5-1 = 4 til pH = 5+1 = 6, men i praksis er omslagsområdet lidt anderledes, da øjet ikke er lige følsomt for begge farver. Omslagsåmrådet for en to-farvet indikator som methylrødt er principelt uafhængig af indikatorkoncentrationen, som det ses af pufferligningen.
For en ensfarvet indikator som phenolphthalein begynder omslaget, når der er dannet så meget af den farvede form, at farven lige akkurat kan ses - dvs. ved en bestemt koncentration af det farvede stof.
Omdannelsesgraden - dvs. forholdet [farvet]/[ufarvet] er kun afhængig af opløsningens pH. Den absolutte koncentration af den farvede form er derimod afhængig af den totale indikatorkoncentration. Derfor bliver phenolphthaleins omslagsområde lidt afhængigt af den valgte indiatorkoncentration, men dette forhold spille dog ingen praktisk rolle i almindelighed.
Ved titrering af stærke syrer med stærke baser (eller omvendt) kan både methylrødt, BTB og phenolphthalein anvendes.
Phenolphthaleins omslagsområde gør imidlertid denne indikator særlig anvendelig ved titrering af svage syrer med stærk base.
